Qual vídeo/vlog vocês querem no canal do youtube?
Pesquisar este blog
Formulário de contato
Seguidores
Google Analytics
A Blogueira

Estudante de Análises Clínicas, formada em técnico em farmácia, técnico em química e atualmente maquiadora profissional, aquariana, 29 anos, adora escrever, adora livros, Potterhead.
Seguidores
Marcadores
- 2015
- ABRASTA.
- ajuda
- Aparelho Ortodôntico
- capricho
- Concurso
- Copra
- Curso
- dentista
- Dicas
- Embelleze
- Escola
- Guerreiros do Ferro
- Jana Taffarel
- Livros
- Lorrayne Mavromatis
- Luiza Gomes
- Mairibel
- Maquiagem
- Material Escolar
- Novex
- Parceria
- Playlist
- Produtos
- Química
- Receitinhas
- Resenha
- Resenhas
- TAG
- Talassemia
- TIF
- Vitay
- Volta ás Aulas
Tecnologia do Blogger.
sexta-feira, 31 de maio de 2013
Sou portadora de Talassemia Major, atualmente tenho 23 anos, estou no último período do Curso Técnico em Farmácia, moro no Paraná, na cidade de Maringá. Moro com minha mãe. Neste post vou contar minha história - como meus pais descobriram que eu tinha talassemia.
Nasci em 1990, era uma criança normal, até aos seis meses, meus pais perceberem que minha pele estava pálida. Decidiram me levar ao pediatra, lá ele fez todos os exames e falou que meu diagnóstico era uma simples anemia fiquei em coma, quase morri.Depois fui encaminhada ao Dr.Giorgio, que enfim descobriu a Talassemia Major.Hoje vivo normalmente,tomo meus remédios (Desferal, ac.fólico..)faço minhas transfusões de sangue. Doem sangue, salvem vidas! Obrigada Deus por tudo!
Nasci em 1990, era uma criança normal, até aos seis meses, meus pais perceberem que minha pele estava pálida. Decidiram me levar ao pediatra, lá ele fez todos os exames e falou que meu diagnóstico era uma simples anemia fiquei em coma, quase morri.Depois fui encaminhada ao Dr.Giorgio, que enfim descobriu a Talassemia Major.Hoje vivo normalmente,tomo meus remédios (Desferal, ac.fólico..)faço minhas transfusões de sangue. Doem sangue, salvem vidas! Obrigada Deus por tudo!

Bom pessoal, praticamente é isso tudo sobre talassemia. A fonte que usei é www.abrasta.org.br
A ABRASTA é a Associação Brasileira dos Talassêmicos, ela dá um grande suporte para os pacientes. Em caso de qualquer dúvida entre em contato com eles.
A ABRASTA é a Associação Brasileira dos Talassêmicos, ela dá um grande suporte para os pacientes. Em caso de qualquer dúvida entre em contato com eles.

Até a década de 60, as pessoas com Talassemia Major morriam antes de chegar à adolescência, pois os benefícios da terapia transfusional em evitar a anemia crônica eram desconhecidos.
Mais tarde, o problema que prevenia muita pessoa com talassemia de alcançar a idade de 20 anos iniciaram-se pelo acúmulo de ferro no organismo, causado através do tempo pelas transfusões e pela própria capacidade do Sistema Gastrointestinal da pessoa com talassemia de absorver o máximo do mineral oriundo da dieta. Este excesso sobrecarregava os órgãos vitais, tais como o coração, causando doenças como insuficiência Cardíaca, que era uma das principais causas.
Na década de 70, com o surgimento dos agentes quelantes, categoria de drogas capaz de "remover" o ferro do sangue e eliminá-lo do organismo, a expectativa de vida das pessoas com talassemia que seguissem estritamente o tratamento baseado em TRANSFUSÕES + AGENTES QUELANTES tornou-se mais similar àquela das outras pessoas saudáveis.
Atualmente, algumas pesquisas recentes apontam uma cura possível da doença, no futuro. Entre as alternativas terapêuticas que tendem a corrigir a fonte do problema no organismo, e encorajar a produção de hemoglobinas saudáveis, encontramos o Transplante de Medula Óssea (TMO), e a terapia gênica. Compreenda abaixo as proposições de cada uma das intervenções:
Mais tarde, o problema que prevenia muita pessoa com talassemia de alcançar a idade de 20 anos iniciaram-se pelo acúmulo de ferro no organismo, causado através do tempo pelas transfusões e pela própria capacidade do Sistema Gastrointestinal da pessoa com talassemia de absorver o máximo do mineral oriundo da dieta. Este excesso sobrecarregava os órgãos vitais, tais como o coração, causando doenças como insuficiência Cardíaca, que era uma das principais causas.
Na década de 70, com o surgimento dos agentes quelantes, categoria de drogas capaz de "remover" o ferro do sangue e eliminá-lo do organismo, a expectativa de vida das pessoas com talassemia que seguissem estritamente o tratamento baseado em TRANSFUSÕES + AGENTES QUELANTES tornou-se mais similar àquela das outras pessoas saudáveis.
Atualmente, algumas pesquisas recentes apontam uma cura possível da doença, no futuro. Entre as alternativas terapêuticas que tendem a corrigir a fonte do problema no organismo, e encorajar a produção de hemoglobinas saudáveis, encontramos o Transplante de Medula Óssea (TMO), e a terapia gênica. Compreenda abaixo as proposições de cada uma das intervenções:
Transplante de Medula Óssea (TMO)
Melhor conhecido como transplante de células tronco hematopoiéticas, (TCTH) – pelo fato de que, diferentemente da maioria dos transplantes, neste caso a pessoa com talassemia recebe, via endovenosa, as células aspiradas da medula óssea do doador. O procedimento, aparentemente simples, tem o objetivo de – no caso da talassemia – inibir a operação da medula óssea da pessoa com talassemia, fazendo com que as células tronco doadas se fixem na medula do receptor, iniciando a se multiplicar, e assim assumido a produção de células do sangue – a qual passa a produzir células com hemoglobina normal.
Os problemas envolvidos são ainda os riscos envolvidos no procedimento, entre os quais o desenvolvimento da doença enxerto versus hospedeiro (GVHD)– mais agressiva do que a própria Talassemia – o que ocorre quando as novas células do sistema imunológico, presentes na medula do doador, (estas células também são produzidas na Medula óssea, juntamente com as células vermelhas ou hemácias, e a tecnologia atual ainda não é capaz de separá-las para transfusão apenas das células tronco produtoras de hemácias) não reconhecem as células do receptor (pessoa com talassemia) e – a partir daí – começam a destruí-las, surgindo então um processo de origem imunológica. Caso este processo ocorra, a pessoa com talassemia necessitará usar medicamentos imunossupressores durante o resto de sua vida, de maneira a conter a evolução das lesões – as quais ocorrem principalmente (mas não somente) na pele, fígado e pulmões.
Um estudo italiano realizado com 1.000 pessoas com talassemia e publicado em 2008 mostrou uma taxa de mortalidade muito alta entre as pessoa com talassemia submetidos ao transplante – variando de 12% a 40%. As mortes foram maiores em pacientes adultos, com idades superiores há 16 anos.
Melhor conhecido como transplante de células tronco hematopoiéticas, (TCTH) – pelo fato de que, diferentemente da maioria dos transplantes, neste caso a pessoa com talassemia recebe, via endovenosa, as células aspiradas da medula óssea do doador. O procedimento, aparentemente simples, tem o objetivo de – no caso da talassemia – inibir a operação da medula óssea da pessoa com talassemia, fazendo com que as células tronco doadas se fixem na medula do receptor, iniciando a se multiplicar, e assim assumido a produção de células do sangue – a qual passa a produzir células com hemoglobina normal.
Os problemas envolvidos são ainda os riscos envolvidos no procedimento, entre os quais o desenvolvimento da doença enxerto versus hospedeiro (GVHD)– mais agressiva do que a própria Talassemia – o que ocorre quando as novas células do sistema imunológico, presentes na medula do doador, (estas células também são produzidas na Medula óssea, juntamente com as células vermelhas ou hemácias, e a tecnologia atual ainda não é capaz de separá-las para transfusão apenas das células tronco produtoras de hemácias) não reconhecem as células do receptor (pessoa com talassemia) e – a partir daí – começam a destruí-las, surgindo então um processo de origem imunológica. Caso este processo ocorra, a pessoa com talassemia necessitará usar medicamentos imunossupressores durante o resto de sua vida, de maneira a conter a evolução das lesões – as quais ocorrem principalmente (mas não somente) na pele, fígado e pulmões.
Um estudo italiano realizado com 1.000 pessoas com talassemia e publicado em 2008 mostrou uma taxa de mortalidade muito alta entre as pessoa com talassemia submetidos ao transplante – variando de 12% a 40%. As mortes foram maiores em pacientes adultos, com idades superiores há 16 anos.
Como achar um doador
Este deve ter uma estrutura antigênica HLA (HLA é a sigla para Human Leukocyte Antigens ou antígenos leucocitários humanos) compatível com o paciente. Estes antígenos têm a função de permitir ao organismo que diferenciem suas próprias substâncias (antígenos) daquelas de organismos, pessoas e agentes estranhos, e portanto realizam uma função fundamental para evitar a rejeição dos transplantes. Então o doador deve ser buscado, primeiro, na família: há uma chance de 25% de encontrar um bom doador entre irmãos filhos de mesmo pai e mãe, e esta é a maior chance encontrada. Quando este doador não é encontrado (60% dos casos), o candidate ao transplante deve recorrer ao Registro Brasileiro de Doadores de Medula Óssea (REDOME), em busca de um doador compatível voluntário. O Transplante de Medula Óssea de doador não relacionado apresenta um risco maior e deve ser mais bem avaliado, considerando todos os riscos e benefícios. Mais informações,clique aqui.
Este deve ter uma estrutura antigênica HLA (HLA é a sigla para Human Leukocyte Antigens ou antígenos leucocitários humanos) compatível com o paciente. Estes antígenos têm a função de permitir ao organismo que diferenciem suas próprias substâncias (antígenos) daquelas de organismos, pessoas e agentes estranhos, e portanto realizam uma função fundamental para evitar a rejeição dos transplantes. Então o doador deve ser buscado, primeiro, na família: há uma chance de 25% de encontrar um bom doador entre irmãos filhos de mesmo pai e mãe, e esta é a maior chance encontrada. Quando este doador não é encontrado (60% dos casos), o candidate ao transplante deve recorrer ao Registro Brasileiro de Doadores de Medula Óssea (REDOME), em busca de um doador compatível voluntário. O Transplante de Medula Óssea de doador não relacionado apresenta um risco maior e deve ser mais bem avaliado, considerando todos os riscos e benefícios. Mais informações,clique aqui.
Porque congelar o cordão umbilical de pessoas com Talassemia?
Porque, se o irmão saudável apresentar um HLA compatível, e a pessoa com talassemia for um candidato ao Transplante de Medula óssea (TMO), as células para o procedimento podem ser tiradas do cordão umbilical congelado.
Porque, se o irmão saudável apresentar um HLA compatível, e a pessoa com talassemia for um candidato ao Transplante de Medula óssea (TMO), as células para o procedimento podem ser tiradas do cordão umbilical congelado.
Dica do especialista
Uma vez que, atualmente, a Talassemia é uma doença benigna, e que pode ser controlada por meio de transfusões, drogas e acompanhamento medico, muitos especialistas são unânimes em não indicar a exposição das pessoas com talassemia – especialmente daqueles que apresentam sobrecarga cardíaca de Ferro – aos riscos do Transplante de Medula óssea (TMO). Contudo, caso a pessoa com talassemia seja uma candidata ao TMO e deseje se submeter ao procedimento, a recomendação é de que o procedimento se dê com um doador compatível com idade inferior a 16 anos, e em um centro altamente especializado na técnica.
Centros especializados em transplantes de coleta de Medula Óssea no Brasil: AMEO - Associação da Medula Óssea
Uma vez que, atualmente, a Talassemia é uma doença benigna, e que pode ser controlada por meio de transfusões, drogas e acompanhamento medico, muitos especialistas são unânimes em não indicar a exposição das pessoas com talassemia – especialmente daqueles que apresentam sobrecarga cardíaca de Ferro – aos riscos do Transplante de Medula óssea (TMO). Contudo, caso a pessoa com talassemia seja uma candidata ao TMO e deseje se submeter ao procedimento, a recomendação é de que o procedimento se dê com um doador compatível com idade inferior a 16 anos, e em um centro altamente especializado na técnica.
Centros especializados em transplantes de coleta de Medula Óssea no Brasil: AMEO - Associação da Medula Óssea
Terapia Gênica ou Genética
Esta técnica permitiria que, através da ajuda de um "vetor" ou transportador (o qual poderia ser, por exemplo, um vírus atenuado ou incapaz de produzir doença) um novo gene – chamado gene terapêutico – seria inserido no organismo do paciente – no caso, de maneira a ser inserido no cromossoma 11 ou 16, de maneira a corrigir a mutação genética que leva à malformação da Hemoglobina, e consequentemente à anemia crônica. O objetivo do procedimento seria possibilitar que, a partir dessa intervenção, a medula óssea começasse a produzir hemoglobinas saudáveis, e dessa maneira a doença desapareceria. Entretanto, o problema é que os poucos estudos realizados com esta terapia em pessoas com talassemia não produziram ainda resultados promissores – tem-se observado que, na prática, ou a doença retorna, ou ocorre o óbito do paciente. Estes estudos ainda estão em fase experimental, mas a ideia é promissora.
Os avanços na área de biotecnologia da década de 1980 tornaram a ideia da Terapia Gênica famosa como sendo a "luz no final do túnel" para diversos pacientes que sofrem de doenças genéticas raras, crônicas e incapacitantes. Infelizmente, a maioria dos pesquisadores aponta que a cura, para algumas doenças, não está tão próxima como alguns cientistas imaginavam – um dos maiores efeitos colaterais apontados tem sido o desenvolvimento de câncer entre os pacientes que se submeteram ao procedimento.
Esta técnica permitiria que, através da ajuda de um "vetor" ou transportador (o qual poderia ser, por exemplo, um vírus atenuado ou incapaz de produzir doença) um novo gene – chamado gene terapêutico – seria inserido no organismo do paciente – no caso, de maneira a ser inserido no cromossoma 11 ou 16, de maneira a corrigir a mutação genética que leva à malformação da Hemoglobina, e consequentemente à anemia crônica. O objetivo do procedimento seria possibilitar que, a partir dessa intervenção, a medula óssea começasse a produzir hemoglobinas saudáveis, e dessa maneira a doença desapareceria. Entretanto, o problema é que os poucos estudos realizados com esta terapia em pessoas com talassemia não produziram ainda resultados promissores – tem-se observado que, na prática, ou a doença retorna, ou ocorre o óbito do paciente. Estes estudos ainda estão em fase experimental, mas a ideia é promissora.
Os avanços na área de biotecnologia da década de 1980 tornaram a ideia da Terapia Gênica famosa como sendo a "luz no final do túnel" para diversos pacientes que sofrem de doenças genéticas raras, crônicas e incapacitantes. Infelizmente, a maioria dos pesquisadores aponta que a cura, para algumas doenças, não está tão próxima como alguns cientistas imaginavam – um dos maiores efeitos colaterais apontados tem sido o desenvolvimento de câncer entre os pacientes que se submeteram ao procedimento.

Números da Talassemia no Brasil
No Brasil, em que a forma mais comum de talassemia é a Beta Talassemia (minor, Intermédia e Major), milhões de pessoas têm o gen da doença – 90% na forma minor, assintomática e sem necessidade de tratamento. Uma vez que a doença pode ser passada de pais para filhos, essas pessoas – ao não saber de sua doença – podem passar a forma mais severa para as gerações futuras.
Talassemia Intermédia: 202
| Região do Brasil | Nº de Casos | % do total de casos |
| Norte | 6 | 2,97% |
| Nordeste | 69 | 34,16% |
| Centro-Oeste | 7 | 3,47% |
| Sudeste | 101 | 50% |
| Sul | 19 | 9,41% |
Talassemia Major: 302
| Região do Brasil | Nº de Casos | % do total de casos |
| Norte | 5 | 1,66% |
| Nordeste | 35 | 11,59% |
| Centro-Oeste | 22 | 7,28% |
| Sudeste | 201 | 66,56% |
| Sul | 39 | 12,91% |

De acordo com uma pesquisa realizada pela ABRASTA em 2009, com 74 pessoas com Talassemia Intermédia e Talassemia Major, representantes de 13 estados do Brasil, a maioria destes relatou que o tratamento depende, não apenas do Hematologista (o médico especializado em doenças que afetam o sangue), mas também da avaliação e monitoração de outros profissionais, especialmente o Cardiologista (o qual foi visitado por 35,62% dos entrevistados). Isto ocorre em virtude das características da doença, as quais inclinam a pessoa com talassemia a certos problemas ou efeitos colaterais do tratamento. Verifique abaixo as principais complicações, porque ocorrem e como evitá-las:
Coração
A sobrecarga de ferro é o maior vilão para este órgão vital, mesmo quando a pessoa com talassemia segue estritamente a terapia de quelação. Isto ocorre porque a verdadeira intensidade do acúmulo do mineral no coração nem sempre é diagnosticada, e a dose do agente quelante administrada pode ser abaixo do ideal. Com os avanços no tratamento, como a modernização dos agentes quelantes – e, consequentemente, a melhor adesão à terapia –, e além disso, com a possibilidade de se realizar o exame de Ressonância Magnética com T2* – o qual revela com precisão a quantidade de ferro acumulada no Coração.-, o risco de uma pessoa com talassemia desenvolver cardiopatia tem sofrido redução. Contudo, mesmo assim uma grande atenção é requerida com este "amigo do peito".
PREVENÇÃO: Como as complicações cardíacas são ainda a maior causa de morte entre as pessoas com talassemia, o acompanhamento periódico com um cardiologista, a partir da adolescência, é essencial – especialmente se o jovem começa a apresentar sinais e sintomas que podem indicar problemas cardíacos, tais como: sensação de tremores, dispneia (dificuldade respiratória), desfalecimento, dor abdominal (particularmente localizada na região logo acima do estômago ou hipocôndrio), cansaço aos menores esforços, edema.
Coração
A sobrecarga de ferro é o maior vilão para este órgão vital, mesmo quando a pessoa com talassemia segue estritamente a terapia de quelação. Isto ocorre porque a verdadeira intensidade do acúmulo do mineral no coração nem sempre é diagnosticada, e a dose do agente quelante administrada pode ser abaixo do ideal. Com os avanços no tratamento, como a modernização dos agentes quelantes – e, consequentemente, a melhor adesão à terapia –, e além disso, com a possibilidade de se realizar o exame de Ressonância Magnética com T2* – o qual revela com precisão a quantidade de ferro acumulada no Coração.-, o risco de uma pessoa com talassemia desenvolver cardiopatia tem sofrido redução. Contudo, mesmo assim uma grande atenção é requerida com este "amigo do peito".
PREVENÇÃO: Como as complicações cardíacas são ainda a maior causa de morte entre as pessoas com talassemia, o acompanhamento periódico com um cardiologista, a partir da adolescência, é essencial – especialmente se o jovem começa a apresentar sinais e sintomas que podem indicar problemas cardíacos, tais como: sensação de tremores, dispneia (dificuldade respiratória), desfalecimento, dor abdominal (particularmente localizada na região logo acima do estômago ou hipocôndrio), cansaço aos menores esforços, edema.
Hormônios
Um dos problemas mais comuns das pessoas com talassemia é que apresentam uma estrutura óssea frágil e delgada, a qual favorece o surgimento precoce da osteoporose. Por trás disto, estão a própria anemia, e a medula óssea hiperativa; mas também o excesso de Ferro no organismo, bem como os problemas endocrinológicos – atraso na puberdade e desenvolvimento sexual, por exemplo – interferem na absorção de Cálcio pelos ossos e, consequentemente, na densidade óssea.
A sobrecarga de ferro no organismo da pessoa com talassemia usualmente tem como alvo certos órgãos produtores de hormônios – o que pode levar, caso a quelação e monitoração destes não seja feita apropriadamente em cada estágio da vida, a um desequilíbrio hormonal capaz de afetar o crescimento, atrasar o início da puberdade, e mesmo causar doenças.
Quando o alvo da terapêutica é...
Hipófise ou Glândula Pituitária
Quando o alvo da terapêutica é...
Hipófise ou Glândula Pituitária
Localizada na base do cérebro, é responsável pela produção de diversos hormônios, entre os quais o GH (Hormônio do Crescimento) e as Gonadotrofinas (homônimos sexuais masculinos e femininos, que se associam com a "revolução" hormonal que marca a chegada da puberdade).
Consequências: Crescimento inferior e atraso no desenvolvimento sexual (hipogonadismo), tal como o baixo desenvolvimento de mamas e testículos.
Tireóide
Consequências: Crescimento inferior e atraso no desenvolvimento sexual (hipogonadismo), tal como o baixo desenvolvimento de mamas e testículos.
Tireóide
Esta glândula se localiza no pescoço, e tem a função de manutenção do ritmo do metabolismo. Dependendo de como é afetada, pode acelerar ou decrescer a "velocidade" das funções orgânicas, resultando respectivamente no Hipertiroidismo (ocorrem taquicardia ou aceleração do coração, alguns casos de diarréia, perda de peso) ou Hipotiroidismo (sonolência, frio, lentidão mental e física, ganho de peso). O acometimento causado pela Talassemia é o hipotireoidismo.
Consequências: Sonolência, frio, lentidão mental e física, ganho de peso.
Pâncreas
Consequências: Sonolência, frio, lentidão mental e física, ganho de peso.
Pâncreas
As células beta do pâncreas são responsáveis pela produção do hormônio Insulina, o qual controla os níveis de glicose (açúcar) no sangue. Caso, por alguma razão, estas células não puderem trabalhar adequadamente, o organismo sente falta desta insulina para induzir o metabolismo da Glicose ingerida (inicialmente, ocorre a intolerância à Glicose). À medida em que o processo progride, a Glicose não poderá penetrar nas células, e começará a se acumular no sangue (Agora, já se trata de Diabetes completamente desenvolvido).
Consequências: De acordo com dados da Fundação Internacional de Talassemia (TIF), aproximadamente a metade das pessoas com talassemia sofrem de intolerância à Glicose, e cerca de 10 a 30% desenvolvem Diabetes Mellitus Tipo 2 em algum momento de suas vidas.
Consequências: De acordo com dados da Fundação Internacional de Talassemia (TIF), aproximadamente a metade das pessoas com talassemia sofrem de intolerância à Glicose, e cerca de 10 a 30% desenvolvem Diabetes Mellitus Tipo 2 em algum momento de suas vidas.
Prevenção: A partir dos 10 anos de vida, uma consulta prévia ao endocrinologista e um check-up, com realização de alguns exames de sangue específicos, podem ser identificados a tempo os problemas mencionados acima.
Ossos
Um dos problemas mais comuns das pessoas com talassemia é que apresentam uma estrutura óssea frágil e delgada, a qual favorece o surgimento precoce da osteoporose. Por trás disto, estão a própria anemia, e a medula óssea hiperativa; mas também o excesso de Ferro no organismo, bem como os problemas endocrinológicos – atraso na puberdade e desenvolvimento sexual, por exemplo – interferem na absorção de Cálcio pelos ossos e, consequentemente, na densidade óssea.

O que são: medicamentos com substâncias ativas capazes de se ligar ao ferro, produzindo assim um composto que pode ser excretado do organismo por meio da urina e/ou das fezes, dependendo da medicação utilizada. Sem a ajuda desses medicamentos, o organismo é incapaz de liberar o excesso de ferro do corpo.
Candidatos à terapia de quelação: pacientes com sobrecarga de ferro secundária a repetidas transfusões de sangue (talassemia, doença falciforme, mielodisplasia, anemias raras)
Quando iniciar a quelação do ferro: após 10-20 transfusões, ou quando os níveis de ferritina (proteína que reflete o estoque de ferro do corpo) estiverem acima de 1000 ng/dL (nanogramas por decilitro de sangue).
Quais os tipos de agentes quelantes: atualmente existem três tipos disponíveis de medicamentos quelantes de ferro para as pessoas com talassemia, cada um representando um marco específico na terapia da talassemia.
Deferoxamine (Desferal): Primeiro agente quelante de ferro disponível no mercado, surgiu na década de 70 e está disponível no SUS. A despeito de sua eficiência em eliminar o ferro do organismo, seu uso encontrou muita resistência entre as pessoas com talassemia porque sua administração é por via subcutânea, com ajuda de uma bomba de infusão, durante 12 a 14 horas contínuas (usualmente à noite, durante o sono), de cinco a sete vezes por semana. O ferro é eliminado pela urina, de modo que ela fica vermelha.
Deferiprone (Ferriprox): Segundo agente quelante de ferro a ser liberado, disponível no Brasil a partir de 2004 e no SUS a partir de 2006. Apresenta vantagens sobre a deferoxamine, entre elas a de ser administrado por via oral. A dose total deve ser dividida em três tomadas ao dia (a cada 8 horas). Os estudos mostram que tem capacidade de eliminar o excesso de ferro do organismo, especialmente do coração. Em alguns casos, a associação de deferoxamine e deferiprone é recomendada para intensificação do tratamento. O ferro é eliminado pela urina, de modo que ela fica vermelha.
Deferasirox (Exjade): É a medicação quelante de ferro mais recente, aprovada no Brasil em 2006 e disponível no SUS desde 2009. Sua administração é por via oral, o comprimido deve ser dissolvido em água ou suco de laranja ou maça e a dose total é administrada apenas uma vez ao dia. Os estudos mostram que é eficiente em eliminar a sobrecarga de ferro no fígado e no coração. Estudos com grande número de pacientes demonstraram sua eficácia em pacientes com talassemia, doença falciforme, mielodisplasia e anemias raras. O ferro é eliminado pelas fezes, de modo que a urina tem coloração normal.
Como a terapia pode ser aplicada: o tratamento quelante de ferro pode ser feito com monoterapia (Desferal ou Ferriprox ou Exjade) ou com terapia combinada (Desferal junto com Ferriprox). Estudo com Exjade em monoterapia demonstra eficácia na quelação do ferro cardíaco. O seu hematologista é quem vai determinar a melhor terapia para você.
De acordo com os especialistas, não há um agente quelante melhor do que os demais, e a escolha da droga ideal para cada pessoa com talassemia deve considerar fatores como efeitos colaterais, quantidade de ferro acumulada no fígado e no coração, estado clínico do paciente, etc. Apenas o médico assistente será capaz de estabelecer o melhor tratamento a seguir e, para ajudá-lo, o Comitê Científico Médico da ABRASTA desenvolveu um protocolo de quelação do ferro (os especialistas podem acessá-lo através da área do site: Suporte aos Médicos, no link Protocolo de tratamento).
Advertência do especialista: A terapia de quelação deve ser indicada e monitorizada por um especialista em Hematologia, de um centro especializado, de maneira a permitir a monitoração periódica com modificação da medicação de acordo com as necessidades
Obtenção via SUS, procedimento:
- O paciente deve procurar a central de atendimento, no local onde faz tratamento, e perguntar onde fica o posto de saúde ou farmácia de alto custo do SUS mais próxima na entrega medicamentos.
- Após essa informação, o paciente deve dirigir-se ao local informado e pedir um formulário que devera ser entregue ao médico que faz tratamento, junto com os outros documentos também solicitados pelo posto.
- Com o formulário preenchido e os documentos em mãos, entregar novamente no posto de saúde ou farmácia de alto custo, sendo entregue um protocolo de confirmação.
- No prazo estimado de 15 a 30 dias, haverá um telegrama informando que o medicamento já esta disponível para retirada.
- No caso de negação do posto ou farmácia de alto custo, a medida cabível é a via judicial.
Havendo a necessidade do judiciário, a parte deve procurar um advogado podendo ser particular ou utilizar-se a Defensoria Publica (para famílias que ganham até três salários mínimos). A ação deve conter o pedido de liminar em caráter de urgência, no qual, o juiz apreciará em de 48 horas. Porém, o autor deve estar manado de alguns documentos como: a negativa do pedido do medicamento por escrito pela Secretaria e um relatório atual e detalhado do seu médico demonstrando a sua necessidade clínica em utilizar o medicamento.
Na maioria das vezes o resultado é positivo, o importante é não desistir.
Na maioria das vezes o resultado é positivo, o importante é não desistir.
Complicações do uso de agentes quelantes de ferro
Tal como qualquer medicamento, os agentes quelantes causam alguns efeitos colaterais que devem ser considerados, já que a pessoa com talassemia periodicamente utiliza este tipo de medicação. Aprenda o que cada uma das três drogas atualmente indicadas para a quelação podem causar a sua saúde, e como se proteger. Vale a pena mencionar que o uso frequente aumenta os riscos de alguns problemas, o que não quer dizer que necessariamente ocorrerão:
Tal como qualquer medicamento, os agentes quelantes causam alguns efeitos colaterais que devem ser considerados, já que a pessoa com talassemia periodicamente utiliza este tipo de medicação. Aprenda o que cada uma das três drogas atualmente indicadas para a quelação podem causar a sua saúde, e como se proteger. Vale a pena mencionar que o uso frequente aumenta os riscos de alguns problemas, o que não quer dizer que necessariamente ocorrerão:
Deferoxamina: Alta frequência de perda ou déficit auditivo, catarata ou redução no crescimento da coluna lombar.
PREVENÇÃO
Avaliação auditiva e exame de fundo de olho anuais. Controle de peso e estatura.
PREVENÇÃO
Avaliação auditiva e exame de fundo de olho anuais. Controle de peso e estatura.
Deferipirona: Neutropenia (redução na quantidade de células brancas ou de defesa), o que pode favorecer infecções oportunistas.
PREVENÇÃO
Realizar um Hemograma a cada 10 dias, interromper o tratamento imediatamente em caso de febre ou sinais de infecção, buscando imediatamente aconselhamento médico.
PREVENÇÃO
Realizar um Hemograma a cada 10 dias, interromper o tratamento imediatamente em caso de febre ou sinais de infecção, buscando imediatamente aconselhamento médico.
Desferasirox: Aumento de creatinina relatado em alguns pacientes
PREVENÇÃO
Execução de exames para avaliar o funcionamento dos rins antes do início do tratamento e, posteriormente, uma vez por mês. Deve-se manter a hidratação adequada e ter cautela principalmente em pacientes que já apresentem alguma alteração renal antes do início do tratamento.
PREVENÇÃO
Execução de exames para avaliar o funcionamento dos rins antes do início do tratamento e, posteriormente, uma vez por mês. Deve-se manter a hidratação adequada e ter cautela principalmente em pacientes que já apresentem alguma alteração renal antes do início do tratamento.

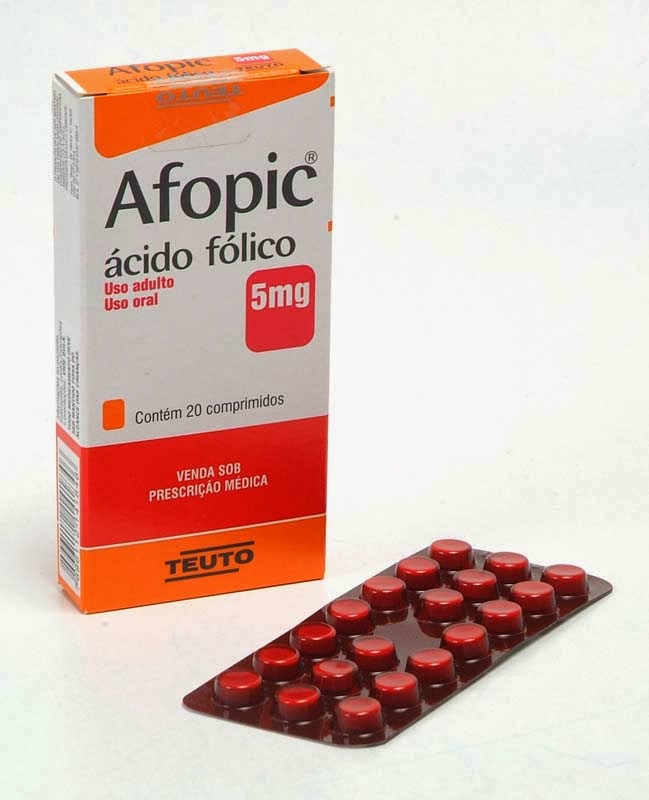
Talassemia Minor: Tratamento: Não há terapia específica. A pessoa deve ficar atenta a situações em que o organismo é submetido a um maior stress, como cirurgia, doenças severas, gravidez nas mulheres. Em alguns casos pode ser necessária a suplementação temporária com ácido fólico (sustância importante na produção das hemácias, células portadoras da hemoglobina).
Também é importante buscar a origem de todas as anemias crônicas que apresentar, mesmo as mais discretas. Por não saber serem portadores desse gene, alguns pacientes podem ser erroneamente diagnosticados e tratados como portadores de anemia carencial.
TRANSFUSÃO SANGUÍNEA + TERAPIA QUELANTE = VIDA NORMAL COM QUALIDADE para pessoas com talassemia major.
Intermediária: Tratamento: Em alguns casos, mesmo após as anemias leves ocasionadas pelo traço talssêmico, a mutação genética presente nestas pessoas causa o desenvolvimento da doença. Usualmente, indivíduos com talassemia minor nunca necessitarão de transfusões ou terapia de quelação,Cheap Cosplay Costumes ao passo que pessoas com talassemia intermédia e major precisarão desses recursos.
Alguns estudos mostraram que, apesar de mais discreta e silenciosa do que nas pessoas com talasssemia major, pessoas com talassemia intermédia usualmente desenvolvem as mesmas complicações. Assim, o regime transfusional pode ser indicado em alguns períodos , por exemplo, durante a infância, caso houver dificuldade de crescimento e risco de deformidades ósseas?ou, em alguns casos, quando o baço e fígado começam a crescer muito e a pessoa começa a desenvolver doenças associadas à talassemia - como diabetes e cardiopatia. Em alguns casos se faz necessária a terapia de quelação.
A talassemia intermédia pode apresentar apenas leve anemia, como o caso da talassemia minor, mas em alguns casos necessita ser tratada como a talassemia major, e é importante monitorizar os níveis de hemoglobina e ferro no sangue. O tratamento é individualizado, e dependerá do status clínico e da história pessoal. Quanto mais velha esta pessoa (mesmo que nunca tenha sofrido transfusões), maior a chance de que seja necessária terapia de quelação.
Também é importante buscar a origem de todas as anemias crônicas que apresentar, mesmo as mais discretas. Por não saber serem portadores desse gene, alguns pacientes podem ser erroneamente diagnosticados e tratados como portadores de anemia carencial.
Major: Tratamento: O paciente com talassemia major deverá ser submetido a transfusões durante toda a vida. A periodicidade usual pode ser de 15, 20 ou 30 dias, de acordo com recomendações médicas. Este processo controla a anemia severa e, caso seja iniciado nos primeiros meses após a descoberta da doença, remove os riscos e complicações que podem afetar o bem-estar e expectativa de vida do indivíduo, tais como deformidades ósseas, hepato-esplenomeglia (aumento do fígado e baço) e insuficiência cardíaca. Aproximadamente após a décima transfusão sucessiva, é necessária uma outra medida: a terapia quelante. Devido às transfusões, a pessoa fica com acúmulo de ferro no organismo. Além disso, o intestino das pessoas com talassemia absorve uma quantidade excessiva pela dieta normal. A quelação elimina este excesso de ferro, através do uso de medicação específica.
TRANSFUSÃO SANGUÍNEA + TERAPIA QUELANTE = VIDA NORMAL COM QUALIDADE para pessoas com talassemia major.
 |
| Exjade - Quelante oral |
 |
| Ferriprox - Quelante Oral |
 |
| Desferal - Quelante Injetável subcutâneo |
 |
| Desferal |
Alguns estudos mostraram que, apesar de mais discreta e silenciosa do que nas pessoas com talasssemia major, pessoas com talassemia intermédia usualmente desenvolvem as mesmas complicações. Assim, o regime transfusional pode ser indicado em alguns períodos , por exemplo, durante a infância, caso houver dificuldade de crescimento e risco de deformidades ósseas?ou, em alguns casos, quando o baço e fígado começam a crescer muito e a pessoa começa a desenvolver doenças associadas à talassemia - como diabetes e cardiopatia. Em alguns casos se faz necessária a terapia de quelação.
A talassemia intermédia pode apresentar apenas leve anemia, como o caso da talassemia minor, mas em alguns casos necessita ser tratada como a talassemia major, e é importante monitorizar os níveis de hemoglobina e ferro no sangue. O tratamento é individualizado, e dependerá do status clínico e da história pessoal. Quanto mais velha esta pessoa (mesmo que nunca tenha sofrido transfusões), maior a chance de que seja necessária terapia de quelação.

Com uma boa investigação e exames ideais, os pais podem saber do diagnóstico de talassemia em seu filho com menos de 1 ano de idade. O ideal é realizar a confirmação diagnóstica entre os três e os seis primeiros meses de vida, de modo que o tratamento – como necessário – inicie logo que possível. Verifique abaixo quais os exames requeridos, quando devem ser feitos e a importância de cada um para a descoberta da doença e a preservação da saúde da pessoa com talassemia.
Hemograma
É o primeiro exame solicitado e serve para, logo no começo, checar se a criança tem anemia ou outra alteração de sangue. Note-se que o hemograma não é específico para a talassemia, podendo ser útil também em outras condições.
Quando fazer: no terceiro mês de vida, particularmente se a criança já apresenta os sinais, como palidez, icterícia (pele e olhos amarelados), sonolência, irritação, choro frequente e dificuldades de sono.
Alerta do Especialista: realizar o hemograma é o primeiro passo, mas para uma possível pessoa com talassemia, este exame não é o suficiente. A talassemia major, por exemplo, inicialmente pode ser tratada como uma anemia comum na infância, o que com certeza prejudica o tratamento futuro. O diagnóstico precoce é essencial para uma melhor qualidade de vida.
Eletroforese de Hemoglobina
Exame de sangue simples e eficiente, é o mais indicado para o diagnóstico da talassemia em crianças com anemias suspeitas. Pode ser feito na maioria dos laboratórios, inclusive de maneira gratuita. Após coleta de 3 – 5 mL de sangue, um processo utilizando eletricidade separa e identifica as hemoglobinas.
Quando fazer: a partir do terceiro mês de vida.
Biologia Molecular
Este exame é mais moderno, e usa técnicas avançadas para identificar com precisão o que causa a má formação da hemoglobina. Na prática, é possível saber não apenas se uma pessoa tem talassemia, mas também qual o tipo. Pode inclusive diagnosticar casos raros de talassemia não identificáveis pela eletroforese.
Quando fazer: dos três aos seis meses de idade.
Hemograma
É o primeiro exame solicitado e serve para, logo no começo, checar se a criança tem anemia ou outra alteração de sangue. Note-se que o hemograma não é específico para a talassemia, podendo ser útil também em outras condições.
Quando fazer: no terceiro mês de vida, particularmente se a criança já apresenta os sinais, como palidez, icterícia (pele e olhos amarelados), sonolência, irritação, choro frequente e dificuldades de sono.
Alerta do Especialista: realizar o hemograma é o primeiro passo, mas para uma possível pessoa com talassemia, este exame não é o suficiente. A talassemia major, por exemplo, inicialmente pode ser tratada como uma anemia comum na infância, o que com certeza prejudica o tratamento futuro. O diagnóstico precoce é essencial para uma melhor qualidade de vida.
Eletroforese de Hemoglobina
Exame de sangue simples e eficiente, é o mais indicado para o diagnóstico da talassemia em crianças com anemias suspeitas. Pode ser feito na maioria dos laboratórios, inclusive de maneira gratuita. Após coleta de 3 – 5 mL de sangue, um processo utilizando eletricidade separa e identifica as hemoglobinas.
Quando fazer: a partir do terceiro mês de vida.
Biologia Molecular
Este exame é mais moderno, e usa técnicas avançadas para identificar com precisão o que causa a má formação da hemoglobina. Na prática, é possível saber não apenas se uma pessoa tem talassemia, mas também qual o tipo. Pode inclusive diagnosticar casos raros de talassemia não identificáveis pela eletroforese.
Quando fazer: dos três aos seis meses de idade.

No Brasil, estima-se que cerca de três milhões de pessoas tenham a talassemia minor, também conhecida por traço talassêmico. Este tipo não apresenta sintomas e não necessita de tratamento.
Alfa: pessoas com alfa talassemia apresentam uma ou mais mutações no cromossomo 16 - afetando a produção das duas cadeias α (alpha) de globina que compõem a hemoglobina. Esta condição pode provocar decréscimo da alfa-globina e sua consequente escassez.
O indivíduo pode ser apenas o portador do gene defeituoso, herdado de um dos pais, sem necessariamente apresentar os sintomas de anemia ou requerer tratamento. Em algumas pessoas com talassemia, nas quais a mutação é leve e afeta apenas ligeiramente a produção de globina, pode ser observada apenas uma leve anemia, necessitando somente de acompanhamento em certas situações, tais como cirurgias, gravidez e idade avançada.
Outra possibilidade é o desenvolvimento da chamada doença da hemoglobina H. Neste caso, o decréscimo da produção de alfa globina é mais grave. As cadeias beta continuam a ser produzidas de maneira normal, e as moléculas excedentes começam a se combinar entre si, originando um novo tipo de hemoglobina – a hemoglobina H. Esta tem uma função semelhante à da hemoglogina normal. Entretanto, como é mais instável, e sua vida (duração) é menor, as células vermelhas (hemácias) que contém esta hemoglobina terão menor duração no organismo, o que resultará em uma anemia de moderada a severa. Se não tratada, suas consequências para o organismo serão fadiga (cansaço), deformações ósseas (pois uma maior parte da medula estará comprometida com a produção das hemácias), e hepatomegalia ou aumento do fígado (o qual estará mais ocupado destruindo as hemácias "velhas"). Para estes pacientes, costuma ser recomendado tratamento à base de transfusões periódicas, em um hemocentro ou hospital especializado, com monitoramento médico periódico e realização de exames anuais. (Veja detalhes em Talassemia MAJOR).
Por outro lado, há casos em que a mutação no cromossomo 16 leva à completa incapacidade do organismo em produzir as cadeias alfa, e a produção de hemoglobina normal torna-se impossível. Este estado produz uma doença conhecida como Hydropsis fetalis, que leva ao óbito do feto ainda no útero. Felizmente este tipo de acontecimento é muito raro.
Beta: As beta-talassemias são mais frequentes no Brasil e no mundo, e pessoas com esta condição apresentam uma ou mais mutações no cromossomo 11. O defeito genético afeta a produção das cadeias beta da hemoglobina, a qual – com as duas cadeias alfa – forma a hemoglobina. A condição genética provoca a redução da produção da beta globina, e sua consequente escassez no organismo. Há uma variedade de subtipos – causadas por uma variedade de cerca de mil mutações já descobertas, mas geralmente se classificam em três grupos básicos: talassemia minor (ou traço talassêmico), intermédia e major.
Talassemia Minor: A talassemia minor é também conhecida como traço talassêmico. Esta pessoa apresenta apenas a herança genética da talassemia – provinda do pai ou da mãe – Na maioria dos casos, apresenta apenas leve anemia, que perdura por toda a vida, mas não traz prejuízo significativo ao organismo nem requer tratamento.
Dica do Especialista: Há exames simples – e oferecidos gratuitamente pelo SUS – que apresentam o metabolismo do ferro no organismo: ferro sérico, saturação da transferrina, ferritina, importantes na avaliação da anemia por carência de ferro, facilitando o diagnóstico das talassemias.
ATENÇÃO: Mesmo que o indivíduo possa viver toda a vida com talassemia minor, sem necessidade de tratamento, existe uma boa razão para que todos tenham este diagnóstico: há uma chance de 25% de que uma criança, filha de pai e mãe portadores dessa forma leve da doença, venha a nascer com Talassemia Major, mais severa e que requer tratamento logo nos primeiros meses de vida. Assim, o pai ou a mãe que tem talassemia minor deve promover o diagnóstico de seu cônjuge (marido ou mulher), de preferência antes de quaisquer decisões sobre planejamento familiar. Dessa maneira, os pais estarão mais atentos, devendo procurar atenção diagnóstica e terapêutica especializadas, para assegurar a qualidade de vida e longevidade de seus filhos.
Talassemia Major: Também conhecida como anemia mediterrânea ou anemia de Cooley, a talassemia major é o tipo mais grave da doença. Sem tratamento apropriado, a pessoa com esta forma de talassemia – herdada tanto do pai como da mãe – desenvolve anemia severa, a qual pode levar a modificações orgânicas e tóxicas, sérias complicações de saúde e até a morte. A severidade do estado anêmico é medida pela dosagem da hemoglobina no sangue. Na pessoa com talassemia, os níveis dessa proteína geralmente são mantidos abaixo de 8 g/dL (em torno de 6 a 7 g/dL), enquanto em um adulto normal os valores variam de 11 a 16 g/dL. O que causa no organismo: A redução ou falta de cadeias beta da globina afeta diretamente a formação da hemoglobina, originando hemácias (células vermelhas do sangue) mais frágeis e de menor duração, e ainda de menor capacidade de carregamento do oxigênio. Usualmente a condição causa anemia crônica, com sintomas clássicos de palidez, fadiga, fraqueza e sonolência. Um outro fator importante: como duas cadeias beta são necessárias para juntar-se a duas cadeias alfa e formar a molécula de hemoglobina normal (α2β2), resulta que as cadeias alfa se acumulam e depositam nas hemácias circulantes, destruindo-as (hemólise). Isto agrava a anemia, e ainda resulta no excesso de bilirrubina (produzida quando o organismo destrói as hemácias mortas). A bilirrubina é responsável pela icterícia (que pode trazer consequências sérias) no feto. Outro sinal importante é a coloração amarelada da pele e dos olhos. Complicações: Quanto mais é adiado o tratamento, maiores as complicações. Para corrigir a anemia crônica severa, o organismo recorre a alguns mecanismos de defesa, que acabam criando outros problemas:
A medula óssea é a responsável pela produção das células do sangue. Ela sofre um aumento de até 30 vezes o seu tamanho normal, de maneira a ser capaz de produzir mais células vermelhas (hemácias), e compensar por seu baixo número no organismo. Com isso, a formação da parte rígida (mineral) dos ossos também é comprometida. Os ossos crescem mais do que o usual, podendo causar deformidades no crânio e face – especialmente arcada dentária superior. Ocorrem também deformidades nos ossos longos, como costelas, e nas vértebras. Os ossos se tornam finos e mais frágeis, tornando o crescimento da criança mais difícil, e aumentam os riscos de fraturas e osteoporose (ossos porosos e frágeis demais). A terapia transfusional evita estes efeitos, pois mantém a hemoglobina em níveis mais elevados e reduz a necessidade de produção pelo próprio corpo.
- O baço e o fígado também aumentam de tamanho. Esses órgãos são capazes de produzir sangue, em condições específicas. São os produtores de sangue no bebê até a 32ª semana da concepção, e progressivamente cedem esta função à medula. Entretanto na talassemia, como o organismo precisa de maior fluxo de sangue, estes órgãos continuam a produzir sangue e sofrem aumento, pois nesta idade têm também outras funções importantes. Eles também estão envolvidos na destruição das hemácias, que na talassemia major"envelhecem" mais rápido.
- O coração tenta compensar o decréscimo da capacidade de hemoglobina (reduzida) em transportar o oxigênio às células e tecidos. Dessa maneira, começa a bater mais rapidamente para acelerar a circulação sanguínea. Este esforço extra causa taquicardia e produz aumento do coração (cardiomegalia), podendo levar, tardiamente, à insuficiência cardíaca.
Talassemia Intermediária: Como o nome sugere, este tipo de talassemia se encontra, em sua gravidade, entre a talassemia minor e a talassemia major. Há pacientes que apresentam níveis diferenciados da doença, às vezes similares a um, às vezes similares ao outro quadro. Em alguns casos, estes pacientes apresentam uma anemia discreta, mas – diferentemente de pacientes com o traço talassêmico – podem requerer terapia transfusional. Outras vezes, as alterações de exames laboratoriais sugerem a talassemia major, mas a hemoglobina se mantém entre 8 e 10 g/dL e o paciente pode viver sem transfusões.
Diferença: Duas importantes características podem atenuar as similaridades e ajudar a confirmar o diagnóstico. A talassemia intermédia é causada por uma mutação que pode ter sido herdada apenas do pai ou da mãe – não de ambos. Adicionalmente, mesmo se uma anemia crônica discreta descarte o uso de transfusões, este paciente precisará de tratamento para uma vida saudável, e em algum ponto da vida deverá requerer o uso de terapia de quelação.
Complicações: Quanto mais é adiado o tratamento, maiores as complicações. Para corrigir a anemia crônica severa, o organismo recorre a alguns mecanismos de defesa, que acabam criando outros problemas:
A medula óssea é a responsável pela produção das células do sangue. Ela sofre um aumento de até 30 vezes o seu tamanho normal, de maneira a ser capaz de produzir mais células vermelhas (hemácias), e compensar por seu baixo número no organismo. Com isso, a formação da parte rígida (mineral) dos ossos também é comprometida. Os ossos crescem mais do que o usual, podendo causar deformidades no crânio e face – especialmente arcada dentária superior. Ocorrem também deformidades nos ossos longos, como costelas, e nas vértebras. Os ossos se tornam finos e mais frágeis, tornando o crescimento da criança mais difícil, e aumentam os riscos de fraturas e osteoporose (ossos porosos e frágeis demais). A terapia transfusional evita estes efeitos, pois mantém a hemoglobina em níveis mais elevados e reduz a necessidade de produção pelo próprio corpo.
- Alterações ósseas: uma medula óssea hiperativa – resultado dos esforços do organismo em produzir mais hemácias (células vermelhas do sangue) e compensar pela anemia - produz deformidades ósseas. Seu crescimento é interrompido e há maior risco de fraturas. Contudo, alguns destes problemas podem ser solucionados através de transfusões de sangue regulares.
Osteoporose: encorajam-se os pacientes a praticar exercícios físicos e a aumentar o cálcio na dieta, de maneira a evitar esta séria doença óssea. Suplementação oral com cálcio e vitamina D são benéficos. O fumo deve ser evitado. Alguns médicos demonstraram o efeito benéfico do uso de bifosfonatos, administrados via oral ou endovenosa. Contudo, estes estudos necessitam ser confirmados. - Hiperatividade ou expansão da medula óssea e ácido fólico: uma vez que a medula óssea de algumas pessoas com talassemia intermédia se exercita intensamente para combater a anemia, através da produção de mais hemácias, o paciente necessita de maior conteúdo de certas vitaminas, principalmente ácido fólico. Um aporte insuficiente de ácido fólico pode agravar a anemia nesses pacientes. O ácido fólico é naturalmente encontrado em alimentos como carne e vegetais. Contudo, um suplemento adicional (geralmente um comprimido por dia) pode ser benéfico.
- Cálculo bilear: pessoas com talassemia intermédia desenvolvem cálculo bilear (colelitíase) mais frequentemente do que o normal. Os cálculos bileares são formados por subprodutos (pigmentos bileares) liberados durante a degradação das hemácias, e acumulados em um órgão anexo ao fígado – a vesícula bilear – onde podem causar obstrução e dor. A presença dos cálculos pode ser confirmada por ultrassonografia e, em alguns casos, a vesícula bilear deve ser removida cirurgicamente.
- Úlceras de membros inferiores: pessoas com talassemia intermédia, principalmente após uma certa idade, usualmente apresentam úlceras nas regiões a nível de tornozelos, com resultado da circulação e oxigenação insatisfatórias. Tais lesões são de difícil tratamento. Contudo, podem ser prevenidas com um tratamento à base de transfusões de sangue periódicas, e outras medidas preventivas, como elevar os pés acima do coração por 1h a 2h diárias, dormir com elevação dos pés da cama, etc. Uma medicação sugerida é o sulfato de zinco, bem como a hidróxiuréia (medicamento que, em alguns pacientes, é capaz de aumentar a produção de hemoglobina fetal - a qual não necessita de cadeias beta), associada ou não à eritropoietina.
- Complicações renais: outros problemas médicos relatados em pacientes com talassemia intermédia são lesões renais que podem resultar do excesso de ácido úrico no organismo. Este é o mais importante produto residual resultante de hiperatividde da medula óssea. A droga alopurinol pode ajudar
- Thrombofilia: pode haver um aumento na tendência a trombose, a qual ocorre quando trombócitos (plaquetas) se acumulam nos vasos sanguíneos, formando agregados ou coágulos que impedem o fluxo sanguíneo normal. Desta forma, reduz-se o afluxo de sangue aos tecidos. Uma contagem de plaquetas regular ajudará o médico a estabelecer a necessidade de prescrever drogas anti-plaquetárias, caso a contagem se apresente alta, ou antiagregantes/ anticoagulantes, caso haja previsão de cirurgia ou ocorrência de trombose.
- Eritropioese extramedular: a produção de hemácias (células vermelhas do sangue) fora das regiões intramedulares. Diferentemente dos pacientes com talassemia major, que recebem transfusão desde os primeiros meses de vida, pacientes com talassemia intermédia não recebem transfusões regularmente, e portanto continuam a produzir hemácias em grandes quantidades, inclusive fora da medula óssea – principalmente nos segmentos ósseos do tórax e região para-espinhal.
A radiografia pode revelar a formação de tecido em massa nessas regiões. Geralmente, esse fenômeno pode ser identificado através de raios X ou outros métodos mais sensíveis, como ressonância magnética. Devem ser controladas através de terapia transfusional, o que suprimirá esta formação de sangue e, consequentemente, as massas formadas. Se ocorrer alguma condição neurológica mais severa, medidas mais ativas como radioterapia podem ser necessárias. Hidroxiuréia tem também sido utilizada, com bons resultados. - Complicações cardíacas e endócrinas: a anemia crônica pode causar problemas cardíacos. Tanto o coração como o fígado podem ser lesados por uma sobrecarga de ferro, e ambas as condições podem ser controladas da maneira descrita para a talassemia major, com terapia de quelação. Na talassemia intermédia, a doença cardíaca geralmente não está relacionada à sobrecarga de ferro.

Ola a todos, esse é meu mais novo blog. Aqui terá todos os assuntos sobre Talassemia, os cuidados, tratamentos, dicas e tudo mais. Bom, muita gente deve estar perguntando, afinal o que é Talassemia?
A Talassemia é uma desordem hereditária (transmitida de pais para filhos) e que comumente produz anemia (a anemia é um sinal / sintoma comum a várias desordens do corpo humano). Portanto, não é contagiosa, e sim provocada por uma falha genética, a qual leva a uma malformação da Hemoglobina. A Hemoglobina é a proteína encontrada nas hemácias (ou células vermelhas) do sangue, sendo a responsável pelo transporte do Oxigênio a todas as células, tecidos e órgãos do corpo humano.
Cada hemácia circulante possui cerca de 300 milhões de moléculas de Hemoglobina. Cada uma destas moléculas, em seu estado normal, é formada por duas cadeias α (alfa) conectadas a duas cadeias β (beta) de globina (α2β2). As Talassemias são caracterizadas como defeitos no processo de sua produção ou Eritropoiese (do gr. Grego erytra = vermelho + poeisis = producção).
Nas pessoas portadoras de Talassemia, ocorre mutação de um ou dois cromossomas específicos (11 e 16); em resposta, a medula óssea para de produzir (ou produz de maneira insuficiente) um dos tipos de cadeia de globina. Assim, o problema no cromossomo 16 se manifesta pela falta de cadeias α (alfa). Resultará uma desproporcionalidade entre o número de cadeias α e β produzidas, e cada hemácia terá menos moléculas de Hemoglobina em seu interior. Este indivíduo terá a Talassemia α, ou α-talassemia. Caso a mutação esteja presente no cromossomo 11, o paciente terá β-talassemia ou talassemia β. Neste caso, a cadeia de globina faltante será a β.
Há, portanto, dois principais tipos de Talassemia Tipos de Talassemia (alfa e beta), mas existem mais de mil mutações conhecidas nesses dois genes. Cada mutação afeta de uma maneira distinta – mais ou menos intense – a Eritropioese, pela redução da produção de uma das moléculas de golbina. Assim, as reações do organismo – bem como as necessidades e os tipos de tratamento necessários – são variáveis de indivíduo a indivíduo.
As Talassemias são conhecidas como "Anemias do Mediterrâneo", pois a maioria dos casos inicialmente identificados ocorreu em famílias residentes próximo do Mar Mediterrâneo, tais como Itália, Grécia, Turquia e Líbano. O nome se origina do grego "thalassa" (mar). Com a globalização, migração e miscigenação entre os povos, casos passaram a ser relatados em todo o mundo.
Antes do conhecimento sobre a determinação genética da Talassemia, esta era conhecida como Anemia de Cooley - tributo ao pediatra Americano Thomas Cooley, o qual foi o primeiro a descrever, em 1927, os sinais clássicos da doença grave mais conhecida como Talassemia Major.
Fonte: www.abrasta.org.br/tipos

Assinar:
Postagens (Atom)